Перелом физиология
Данная монография о проблемах остеопороза вышла в свет в 2009 году. Пензенский профессор Виллорий Струков более полувека исследовал больных остеопорозом и изложил в работе свои взгляды на поистине мировую проблему потери человеком костной массы, перечислил методы лечения остеопороза, известные миру препараты. Эта работа была написана до того, как компания «Парафарм» выпустила препарат «Остеомед», который совместно разработали ученые — профессор В.И. Струков и физиолог В.Н. Трифонов.
Виллорий Иванович — постоянный участник и лектор всемирных конгрессов по костным заболеваниям. В своей врачебной практике он использовал различные способы лечения остеопороза и переломов, в том числе импортными препаратами — к примеру, американским «Цитракалом». Тем не менее, сегодня профессор Струков говорит о том, что «Остеомед» превзошел его ожидания, так как при его приеме скорость восстановления костной ткани гораздо выше импортных препаратов. А чем быстрее реабилитация человека, тем выше вероятность предотвратить повторный перелом.
С 2009 года Виллорий Иванович начал применять в своей врачебной практике «Остеомед». Результат — на сегодняшний день более чем у 10 тысяч его пациентов не наблюдались повторные переломы. Надо заметить, что такой заслуги нет ни у одного иностранного лекарственного препарата, предназначенного для лечения остеопороза.
«Актуальные проблемы остеопороза».
Монография
под редакцией
профессора, доктора медицинских наук,
зав. кафедрой педиатрии ГОУ ДПО
Пензенского института усовершенствования врачей
В.И. Струкова.
Авторский состав:
В. И. Струков,
М. Ю. Сергеева-Кондраченко,
О. В. Струкова-Джоунс,
Р. Т. Галеева, Л. Г. Радченко,
М. Н. Гербель, Е. Б. Шурыгина,
Л. Д. Романовская, Н. В. Еремина,
Н. А. Вирясова.
Рецензенты:
Л. М. Житникова, д.м.н., профессор кафедры семейной медицины
ММА им. И.М. Сеченова,
исполнительный директор Общероссийской Ассоциации
врачей общей практики.
В. А.Кельцев, д.м.н., профессор,
заведующий кафедрой факультетской педиатрии
ГОУ ВПО Самарского медицинского университета.
Типография «Ростра», 2009. с.342
Костная ткань представляет собой динамическую метаболически активную систему с сопряженными процессами резорбции и новообразования. В течение жизни костная ткань постоянно подвергается моделированию (росту, образованию вновь) в детском возрасте и ремоделированию (перестройке) во взрослом состоянии. Процесс обновления кости рассматривается в настоящее время с позиции теории интермедиарной организации скелета, ключевым понятием которой является «базисная мультиклеточная единица» — БМЕ — участок костной ткани, в котором при сотрудничестве различных типов клеток происходит сопряженный процесс роста и разрушения кости. В организме насчитывается примерно 10 млн таких единиц, состоящих из остеокластов, остеобластов, остеоцитов, макрофагов и моноцитов — предшественников остеокластов, клеток стромы — предшественников остеобластов Дамбахер М. А., Шахт Е., Франке Ю., Рунге Г. 2005 г.).
Скелет человека состоит на 20-25% из трабекулярной кости и на 75-80% из кортикальной (Рис.1). Кортикальная кость формирует диафизы трубчатых костей, имеет плотное строение, выполняет функцию опоры для мышечной ткани и служит для передачи мышечного сокращения. Трабекулярная кость состоит из костных пластинок толщиной 100-150 микрон, она формирует костные эпифизы и аксиальный скелет, ее основная функция состоит в обеспечении нормальной жизнедеятельности костного мозга и костной ткани.
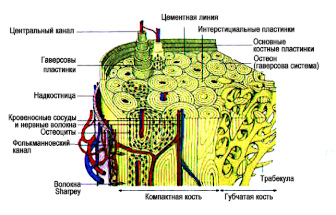
Рис.1. Схема строения длиной кости на продольном и поперечном срезе
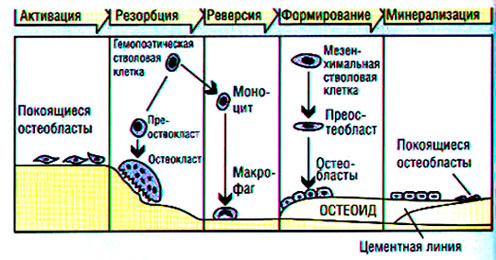
Ежегодно 10-25% скелета взрослого человека подвергается ремоделированию, причем в трабекулярной кости процессы метаболизма происходят быстрее. Костный кругооборот происходит в базисных мультиклеточных единицах — БМЕ (Рис .2, 3) и протекает стадийно: активация — резорбция — переходный период — образование костной ткани — минерализация (Parfit A. M., Chir M. D., Rasmussen H. еt al., Коровина Н. А., Захарова И. Н., Марченкова Л. А; Рожинская Л. Я.).
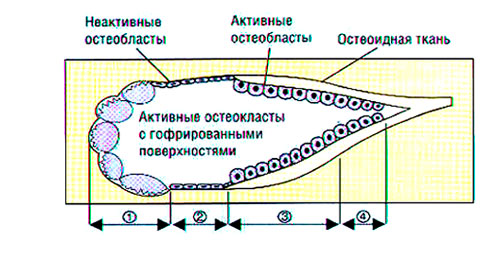
Рис. 2. Схема строения костной единицы ремоделирования (базисная мультиклеточная единица): 1.Остеобластная резорбция. 2.Фаза реверсии. 3.Формирования кости. 4. Минерализация остеоидной ткани
В фазу активации происходит пролиферация предшественников остеокластов в гемопоэтической ткани. Зрелые активированные остеокласты прикрепляются к поверхности резорбируемых участков и в течение 1-3 недель подвергают расплавлению неорганический матрикс, после чего органические элементы деградируют и фагоцитируются. Процесс резорбции происходит с обязательным поступлением в рассасываемый участок ионов водорода, углекислого газа и лизосомальных ферментов остеокластов. Углекислый газ, превращаясь в угольную кислоту, создает локальный ацидоз, способствующий разрушению солей кальция. В переходной фазе происходит созревание предшественников остеобластов, которые спустя 4-6 недель после начала резорбции откладывают в образованные полости костный матрикс со скоростью 2-3 мкм/день.

Рис.3. Цикл ремоделирования кости по Raisz L. G. (1988)
Главным составляющим органического матрикса является синтезируемый остеобластами фибриллярный белок коллаген, в значительной степени определяющий эластичность кости. В небольших количествах в органическом костном матриксе содержатся неколлагеновые белки — гликопротеины, сиалопротеины, альбумины, а также мукополисахариды, гликоген, органические кислоты, липиды.
После заполнения костных дефектов остеобласты превращаются в покоящиеся остеоциты, лежащие в костных лакунах, и формируют выстилающий слой, отделяющий костную поверхность от сосудов. В количественном отношении остеоциты преобладают, эти клетки принимают активное участие в постоянном обмене минеральных и органических компонентов между костным матриксом и тканевой жидкостью, фильтруемой из сосудов (Parfitt A. M.).
Образованный остеобластами коллаген подвергается минерализации, при этом часть кости формируют кристаллы гидроксиапатита, а другая представлена аморфным фосфатом кальция (АФК). Образовавшийся АФК становится источником ионов кальция и фосфора, поскольку аморфный кальций более растворим, чем гидроксиапатит. Механизм превращения АФК в гидроксиапатит является до конца не изученным. Возможно, при этом происходит растворение и гидратация ионов твердой поверхности АФК, передвижение образовавшихся гидратированных ионов и последующий рост кристаллов гидроксиаппатита (Parfitt A. M.).
Всего на долю кальция фосфата приходится в аморфной и кристаллической формах до 85% минеральной массы кости, кальция карбоната 10%, кальция фторида 0.3%, кальция хлорида 0.2%, магния фосфата — 1%, щелочных солей — 2%. Кроме того, в костной ткани присутствуют в незначительных количествах ионы цинка, кремния, алюминия, бария: бериллия, меди и других микроэлементов. Процесс минерализации костного матрикса занимает 5-10 дней. Полностью костеобразование длится около трех месяцев, а полный цикл обновления в каждом участке занимает 4-8 месяцев. (Huffer W. F., цитир. В. И. Струков, 2004 г.).
В основе остеопоротических изменений в костях важная роль принадлежит нарушениям в гормональной регуляции ремоделирования. В результате воздействия эндогенных и экзогенных факторов риска остеопороза происходят сложные нарушения в регулировании метаболизма костной ткани. Особенно значительные нарушения происходят в следующих гормонах:
- паратгормон (стимулятор резорбции);
- тироксин (стимулятор резорбции);
- эстрогены (ингибиторы резорбции);
- кальцитонин (ингибитор резорбции);
- гормон D (минерализация костей);
- медиаторы (цитокины, факторы роста).
Все эти соединения имеют огромное значение в метаболизме кальция. Са – особый минерал. В отличие от сотен тысяч органических соединений, которые организм может производить сам, источником минералов является внешняя среда. Все минералы важны для нормальной работы организма, однако кальций занимает среди них особое место. Его содержание в организме превышает содержание всех остальных минералов и составляет около 2% массы тела. Са участвует более чем в 300 жизненно важных реакциях организма. Соли кальция обеспечивают прочность костей. Без кальция невозможна работа сердца и сосудов, сокращение мышц, деятельность головного мозга и нервной системы и т.д. 99% кальция находится в костях, обеспечивая их прочность, и лишь 1% — в крови, клетках и других биологических жидкостях. Нарушения в кальциевом обмене являются одной из важной причиной нарушения ремоделирования костной ткани, что ведет к резкой активации остеокластов и преобладанию процессов разрушения кости над ее созиданием. Это обстоятельство ведет в конечном счете к изменению морфологии и качества кости, что является причиной её переломов, нередко от небольшой травмы.
Основные патофизиологические механизмы переломов костей при остеопорозе представлены на рис. 4.
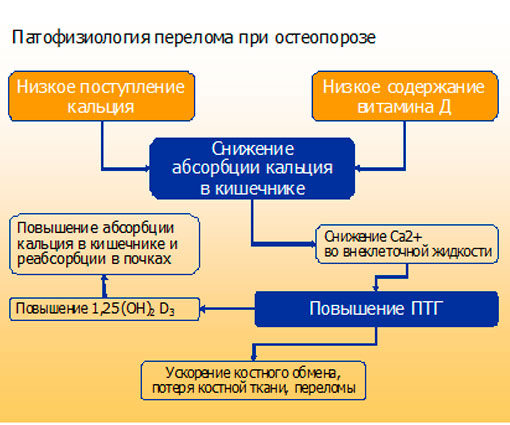
Рис.4. Патофизиологические механизмы развития переломов
Как видно, решающее значение в развитии остеопороза и переломов имеют низкое поступление кальция с пищей, гиповитаминоз D. Это обуславливает снижение абсорбции кальция в кишечнике, развитие гипокальциемии и, как следствие, повышенной продукции паратгормона (ПТГ). Последний обуславливает потерю костной ткани и их переломы.
- Актуальные проблемы остеопороза. Монография
- Актуальные проблемы остеопороза. Список сокращений
- Актуальные проблемы остеопороза. Монография В.И. Струкова. Введение
- Актуальные проблемы остеопороза. Часть I. Физиология костной ткани и патфизиология костных переломов. В. И. Струков
- Актуальные проблемы остеопороза. Часть II. Факторы риска остеопороза. В.И. Струков
- Актуальные проблемы остеопороза. Часть II. Факторы риска остеопороза. В.И. Струков
- Актуальные проблемы остеопороза. Часть III. Классификация остеопороза. Клинические варианты остеопороза, определение. В.И. Струков
- Актуальные проблемы остеопороза. Часть IV. Вторичный остеопороз
- Актуальные проблемы остеопороза. Часть V. Диагностика остеопороза
- Актуальные проблемы остеопороза. Часть VI. Остеопения и остеопороз у детей и подростков
- Актуальные проблемы остеопороза. Часть VII. Профилактика и лечение остеопороза
- Актуальные проблемы остеопороза. Заключение
Источник
Данная монография о проблемах остеопороза вышла в свет в 2009 году. Пензенский профессор Виллорий Струков более полувека исследовал больных остеопорозом и изложил в работе свои взгляды на поистине мировую проблему потери человеком костной массы, перечислил методы лечения остеопороза, известные миру препараты. Эта работа была написана до того, как компания «Парафарм» выпустила препарат «Остеомед», который совместно разработали ученые — профессор В.И. Струков и физиолог В.Н. Трифонов.
Виллорий Иванович — постоянный участник и лектор всемирных конгрессов по костным заболеваниям. В своей врачебной практике он использовал различные способы лечения остеопороза и переломов, в том числе импортными препаратами — к примеру, американским «Цитракалом». Тем не менее, сегодня профессор Струков говорит о том, что «Остеомед» превзошел его ожидания, так как при его приеме скорость восстановления костной ткани гораздо выше импортных препаратов. А чем быстрее реабилитация человека, тем выше вероятность предотвратить повторный перелом.
С 2009 года Виллорий Иванович начал применять в своей врачебной практике «Остеомед». Результат — на сегодняшний день более чем у 10 тысяч его пациентов не наблюдались повторные переломы. Надо заметить, что такой заслуги нет ни у одного иностранного лекарственного препарата, предназначенного для лечения остеопороза.
«Актуальные проблемы остеопороза».
Монография
под редакцией
профессора, доктора медицинских наук,
зав. кафедрой педиатрии ГОУ ДПО
Пензенского института усовершенствования врачей
В.И. Струкова.
Авторский состав:
В. И. Струков,
М. Ю. Сергеева-Кондраченко,
О. В. Струкова-Джоунс,
Р. Т. Галеева, Л. Г. Радченко,
М. Н. Гербель, Е. Б. Шурыгина,
Л. Д. Романовская, Н. В. Еремина,
Н. А. Вирясова.
Рецензенты:
Л. М. Житникова, д.м.н., профессор кафедры семейной медицины
ММА им. И.М. Сеченова,
исполнительный директор Общероссийской Ассоциации
врачей общей практики.
В. А.Кельцев, д.м.н., профессор,
заведующий кафедрой факультетской педиатрии
ГОУ ВПО Самарского медицинского университета.
Типография «Ростра», 2009. с.342
Костная ткань представляет собой динамическую метаболически активную систему с сопряженными процессами резорбции и новообразования. В течение жизни костная ткань постоянно подвергается моделированию (росту, образованию вновь) в детском возрасте и ремоделированию (перестройке) во взрослом состоянии. Процесс обновления кости рассматривается в настоящее время с позиции теории интермедиарной организации скелета, ключевым понятием которой является «базисная мультиклеточная единица» — БМЕ — участок костной ткани, в котором при сотрудничестве различных типов клеток происходит сопряженный процесс роста и разрушения кости. В организме насчитывается примерно 10 млн таких единиц, состоящих из остеокластов, остеобластов, остеоцитов, макрофагов и моноцитов — предшественников остеокластов, клеток стромы — предшественников остеобластов Дамбахер М. А., Шахт Е., Франке Ю., Рунге Г. 2005 г.).
Скелет человека состоит на 20-25% из трабекулярной кости и на 75-80% из кортикальной (Рис.1). Кортикальная кость формирует диафизы трубчатых костей, имеет плотное строение, выполняет функцию опоры для мышечной ткани и служит для передачи мышечного сокращения. Трабекулярная кость состоит из костных пластинок толщиной 100-150 микрон, она формирует костные эпифизы и аксиальный скелет, ее основная функция состоит в обеспечении нормальной жизнедеятельности костного мозга и костной ткани.
Рис.1. Схема строения длиной кости на продольном и поперечном срезе
Ежегодно 10-25% скелета взрослого человека подвергается ремоделированию, причем в трабекулярной кости процессы метаболизма происходят быстрее. Костный кругооборот происходит в базисных мультиклеточных единицах — БМЕ (Рис .2, 3) и протекает стадийно: активация — резорбция — переходный период — образование костной ткани — минерализация (Parfit A. M., Chir M. D., Rasmussen H. еt al., Коровина Н. А., Захарова И. Н., Марченкова Л. А; Рожинская Л. Я.).
Рис. 2. Схема строения костной единицы ремоделирования (базисная мультиклеточная единица): 1.Остеобластная резорбция. 2.Фаза реверсии. 3.Формирования кости. 4. Минерализация остеоидной ткани
В фазу активации происходит пролиферация предшественников остеокластов в гемопоэтической ткани. Зрелые активированные остеокласты прикрепляются к поверхности резорбируемых участков и в течение 1-3 недель подвергают расплавлению неорганический матрикс, после чего органические элементы деградируют и фагоцитируются. Процесс резорбции происходит с обязательным поступлением в рассасываемый участок ионов водорода, углекислого газа и лизосомальных ферментов остеокластов. Углекислый газ, превращаясь в угольную кислоту, создает локальный ацидоз, способствующий разрушению солей кальция. В переходной фазе происходит созревание предшественников остеобластов, которые спустя 4-6 недель после начала резорбции откладывают в образованные полости костный матрикс со скоростью 2-3 мкм/день.
Рис.3. Цикл ремоделирования кости по Raisz L. G. (1988)
Главным составляющим органического матрикса является синтезируемый остеобластами фибриллярный белок коллаген, в значительной степени определяющий эластичность кости. В небольших количествах в органическом костном матриксе содержатся неколлагеновые белки — гликопротеины, сиалопротеины, альбумины, а также мукополисахариды, гликоген, органические кислоты, липиды.
После заполнения костных дефектов остеобласты превращаются в покоящиеся остеоциты, лежащие в костных лакунах, и формируют выстилающий слой, отделяющий костную поверхность от сосудов. В количественном отношении остеоциты преобладают, эти клетки принимают активное участие в постоянном обмене минеральных и органических компонентов между костным матриксом и тканевой жидкостью, фильтруемой из сосудов (Parfitt A. M.).
Образованный остеобластами коллаген подвергается минерализации, при этом часть кости формируют кристаллы гидроксиапатита, а другая представлена аморфным фосфатом кальция (АФК). Образовавшийся АФК становится источником ионов кальция и фосфора, поскольку аморфный кальций более растворим, чем гидроксиапатит. Механизм превращения АФК в гидроксиапатит является до конца не изученным. Возможно, при этом происходит растворение и гидратация ионов твердой поверхности АФК, передвижение образовавшихся гидратированных ионов и последующий рост кристаллов гидроксиаппатита (Parfitt A. M.).
Всего на долю кальция фосфата приходится в аморфной и кристаллической формах до 85% минеральной массы кости, кальция карбоната 10%, кальция фторида 0.3%, кальция хлорида 0.2%, магния фосфата — 1%, щелочных солей — 2%. Кроме того, в костной ткани присутствуют в незначительных количествах ионы цинка, кремния, алюминия, бария: бериллия, меди и других микроэлементов. Процесс минерализации костного матрикса занимает 5-10 дней. Полностью костеобразование длится около трех месяцев, а полный цикл обновления в каждом участке занимает 4-8 месяцев. (Huffer W. F., цитир. В. И. Струков, 2004 г.).
В основе остеопоротических изменений в костях важная роль принадлежит нарушениям в гормональной регуляции ремоделирования. В результате воздействия эндогенных и экзогенных факторов риска остеопороза происходят сложные нарушения в регулировании метаболизма костной ткани. Особенно значительные нарушения происходят в следующих гормонах:
- паратгормон (стимулятор резорбции);
- тироксин (стимулятор резорбции);
- эстрогены (ингибиторы резорбции);
- кальцитонин (ингибитор резорбции);
- гормон D (минерализация костей);
- медиаторы (цитокины, факторы роста).
Все эти соединения имеют огромное значение в метаболизме кальция. Са – особый минерал. В отличие от сотен тысяч органических соединений, которые организм может производить сам, источником минералов является внешняя среда. Все минералы важны для нормальной работы организма, однако кальций занимает среди них особое место. Его содержание в организме превышает содержание всех остальных минералов и составляет около 2% массы тела. Са участвует более чем в 300 жизненно важных реакциях организма. Соли кальция обеспечивают прочность костей. Без кальция невозможна работа сердца и сосудов, сокращение мышц, деятельность головного мозга и нервной системы и т.д. 99% кальция находится в костях, обеспечивая их прочность, и лишь 1% — в крови, клетках и других биологических жидкостях. Нарушения в кальциевом обмене являются одной из важной причиной нарушения ремоделирования костной ткани, что ведет к резкой активации остеокластов и преобладанию процессов разрушения кости над ее созиданием. Это обстоятельство ведет в конечном счете к изменению морфологии и качества кости, что является причиной её переломов, нередко от небольшой травмы.
Основные патофизиологические механизмы переломов костей при остеопорозе представлены на рис. 4.
Рис.4. Патофизиологические механизмы развития переломов
Как видно, решающее значение в развитии остеопороза и переломов имеют низкое поступление кальция с пищей, гиповитаминоз D. Это обуславливает снижение абсорбции кальция в кишечнике, развитие гипокальциемии и, как следствие, повышенной продукции паратгормона (ПТГ). Последний обуславливает потерю костной ткани и их переломы.
- Актуальные проблемы остеопороза. Монография
- Актуальные проблемы остеопороза. Список сокращений
- Актуальные проблемы остеопороза. Монография В.И. Струкова. Введение
- Актуальные проблемы остеопороза. Часть I. Физиология костной ткани и патфизиология костных переломов. В. И. Струков
- Актуальные проблемы остеопороза. Часть II. Факторы риска остеопороза. В.И. Струков
- Актуальные проблемы остеопороза. Часть II. Факторы риска остеопороза. В.И. Струков
- Актуальные проблемы остеопороза. Часть III. Классификация остеопороза. Клинические варианты остеопороза, определение. В.И. Струков
- Актуальные проблемы остеопороза. Часть IV. Вторичный остеопороз
- Актуальные проблемы остеопороза. Часть V. Диагностика остеопороза
- Актуальные проблемы остеопороза. Часть VI. Остеопения и остеопороз у детей и подростков
- Актуальные проблемы остеопороза. Часть VII. Профилактика и лечение остеопороза
- Актуальные проблемы остеопороза. Заключение
