Нарушение сращения переломов


Консолидация костных отломков после перелома происходит по биологическим законам, через определенные временные сроки и зависит от многих факторов.
К местным факторам, способствующим консолидации относятся:
- 1 – точная репозиция костных отломков (устранение смещения),
- 2 – правильно выполненная и достаточная по времени иммобилизация,
- 3 – адекватное кровоснабжение костных фрагментов,
- 4 – ранняя функция при сохранении стабильной фиксации.
Нарушения процессов консолидации обусловлены как внешними факторами (несоблюдение сроков и правил иммобилизации, отклонения в режимах клинического ведения пациентов), так и внутренними (нарушения минерального, белкового, гормонального обменов). Они ведут к замедлению сращения переломов. Развивается процесс неполноценной консолидации или патологическая репаративная регенерация.
Процесс остеорепарации значительно ускоряется при использовании стабильной фиксации костных отломков и хорошем кровообращении. В тех случаях, когда сохраняется подвижность отломков, происходит микротравматизация капиллярной сети и пролиферация тканей, устойчивых к гипоксии,– волокнистой соединительной и хрящевой. Это обстоятельство может привести к рубцовой интерпозиции в зоне перелома, замедленной консолидации и образованию ложного сустава. Важным фактором сращения перелома кости является состояние местного кровообращения.

При переломах повреждаются не только сосуды окружающих мягких тканей, но и сосуды, проходящие в самой кости. В области метафизов костей, где большой мышечный массив, кровоснабжение, как правило, хорошее. Поэтому переломы этой локализации хорошо срастаются. Однако нижняя треть большеберцовой кости, локтевая кость и некоторые другие при переломе могут быть лишены кровоснабжения, так как повреждается внутрикостная артерия, которая является основным источником питания.
Замедленная консолидация переломов

Подробнее…
В тех случаях, когда по истечении максимального срока, необходимого для сращения перелома данной локализации, консолидация не наступает – говорят о замедленной консолидации. При этом отмечается задержка в перестройке фиброзной мозоли в костную.Данный патологический процесс может продолжаться в течение 1,5–2 сроков, необходимых для сращения перлома. Клинически отмечается незначительная эластическая подвижность в месте перелома, боль при нагрузке. Рентгенологические признаки косной мозоли недостаточно выражены, хорошо прослеживается линия перелома.
Лечение замедленной консолидации может быть консервативным и оперативным. Консервативное лечение состоит в продлении иммобилизации перелома на срок, необходимый для его сращения, как если бы он был свежим.
При правильном клиническом ведении пациента после выявления признаков замедленной консолидации, коррекции и применении дополнительной стимуляции регенерации (смена метода фиксации перелома, «игра» с регенератом по типу чередования компрессии и дистракции при лечении методом ВКДО), использование медикаментозных средств (анаболических препаратов, препаратов кальция с витамином D), лазерои магнитотерапии, ультразвуковой стимуляции, клеточных технологий – стимуляция регенерации путём введения в костную мозоль остеобластных клеток – происходит сращение перелома.
При лечении замедленной консолидации необходимо учитывать, что длительное отсутствие функциональной нагрузки на травмированный сегмент приводит к стойкой мышечной атрофии, ограничению подвижности в иммобилизированных суставах. Эти нарушения даже при сращении перелома потребуют очень длительного реабилитационного периода.
Поэтому попытки консервативного лечения при замедленной консолидации оправданы только тогда, когда клинически и рентгенологически процесс консолидации хорошо прослеживается, но ещё не завершен. Если прогнозируемые сроки консолидации увеличиваются более чем на 1–1,5 месяца, предпочтительно оперативное лечение.
Способы оперативного лечения замедленной консолидации:
- 1. Туннелизация по Беку. Спицей Киршнера или сверлом малого диаметра формируют в различных направлениях каналы, проходящие через линию перелома от одного отломка в другой. По этим каналам прорастают сосуды, что способствует сращению перелома.
- 2. Внеочаговый компрессионно-дистракционный остеосинтез (ВКДО) позволяет долгое время прочно удерживать отломки при плотном их соприкосновении, а так же выполнять попеременно компрессию и дистракцию регенерата. Чаще используют аппарат Илизарова.
- 3. Стабильно-функциональный погружной остеосинтез с использованием интрамедуллярных фиксаторов с блокированием. Этот метод допускает раннюю функциональную нагрузку сегмента до полной костной консолидации. Использование накостного остеосинтеза пластинами LCP – пластины с ограниченным контактом.
- 4. Костная пластика.
Ложные суставы
Ложный сустав – это стойкое нарушение целостности кости, имеющее клинические и рентгенологические признаки. Если консолидация перелома не состоялась в более чем двойной срок сращения для данной локализации и произошло закрытие костномозговых каналов, можно констатировать формирование ложного сустава.
Клинические признаки: патологическая подвижность на уровне повреждения, боль в области ложного сустава, изменение анатомической оси сегмента конечности. Рентгенологически – отчетливо определяется линия ложного сустава между отломками, склероз или остеопороз концов отломков, формирование «замыкательных» пластинок, закрывающих костномозговые каналы, как на проксимальном, так и на дистальном отломках.
Таким образом, проксимальный и дистальный фрагменты закрыты зонами склерозированной ткани, которая является непреодолимым препятствием для пролиферации клеток эндоста, периоста и костного мозга. Поэтому клинический диагноз «ложный сустав» указывает на невозможность достичь консолидации консервативными методами.
Различают нормотрофический, гипертрофический, гипотрофический, атрофический, истинный фиброзно-синовиальный ложный сустав (неоартроз).
В нормотрофическом ложном суставе сохраняются процессы формирования костной мозоли, но они протекают больше двойного срока сращения для данной локализации.
В гипертрофическом ложном суставе идет усиленное костеобразование, которое сопровождается образованием избыточной костной мозоли, узкой плохо прослеживаемой линией ложного сустава.
В гипотрофическом и атрофическом ложных суставах превалируют процессы рассасывания костных отломков в области перелома, отмечается выраженный остеопороз и атрофия костной ткани, сохраняется достаточно выраженная подвижность в области ложного сустава, боль. Крайняя степень выраженности атрофии – «болтающийся» ложный сустав – встречается при огнестрельных переломах, при первичных травматических дефектах костной ткани.
Признаки истинного фиброзно-синовиального ложного сустава (неоартроза):
- 1) сглаженность и закругленность обоих костных отломков с полным закрытием костномозговых каналов,
- 2) развитие соединительной ткани и хряща на концах поврежденной кости,
- 3) формирование соединительнотканной «сумки» в области перелома наподобие капсулы сустава, заполненной жидкостью, сходной с синовиальной,
- 4) сохранение практически безболезненной подвижности костных фрагментов,
- 5) неопороспособность конечности.
Лечение
В лечении ложных суставов сочетают консервативные и оперативные методы. К консервативным способам лечения относят физиотерапевтические методы: электростимуляция образования костной мозоли, волновое лечение (лазеротерапия, магнитотерапия, светотерапия, теплотерапия), медикаментозное лечение, оптимизирующее минеральный баланс. Нередко применяют анаболические стероиды, которые стимулируют все виды обменов.
При оперативном лечении ложных суставов могут быть использованы все методы, изложенные в разделе хирургического лечения замедленной консолидации.
Оперативные методы делят на очаговые (с вмешательством на патологичесой зоне) и внеочаговые (без вмешательства). К внеочаговым относят применение аппаратов внешней фиксации. При использовании аппаратов внешней фиксации после его наложения чередуют дистракцию и компрессию, а затем стабилизируют аппарат. Как правило, нормотрофические и гипертрофические ложные суставы лечатся без вмешательства на очаге аппаратным остеосинтезом и консервативными методами.
Оперативное лечение с вмешательством на очаге бывает нескольких видов: малоинвазивное и инвазивное. К малоинвазивным методикам относят введение остеогенных материалов (костного матрикса) или остеогенных клеток (остеобластных и стволовых) в костную мозоль либо параоссально в проекции ложного сустава.
Из инвазивных методов применяется декортикация костных концов отломков с резекцией патологической зоны и обязательным восстановлением костномозгового канала. Декортикация производится в области концов костных отломков путём отсечения пластинок кортикальной кости с сохранением их связи с окружающими мягкими тканями. Фрагменты отщеплённого кортикального слоя служат дополнительными стимуляторами костеобразования. При образовании костного дефекта он замещается костными трансплантатами. Фиксация кости осуществляется погружными металлическими конструкциями, либо аппаратами внешней фиксации.
Сроки восстановления, как правило, превышают в два – три раза средние сроки характерные для сращения переломов данной локализации.
КОСТНАЯ ПЛАСТИКА
Костная пластика – это оперативное вмешательство, направленное на восстановление целостности кости, с использованием костно-пластических материалов. В зависимости от разновидности костно-пластических материалов костную пластику подразделяют на: аутопластику, аллопластику, ксенопластику (гетеропластику), брефопластику и комбинированную пластику.
Костная пластика выполняется различными материалами: аутопластика – использование тканей самого пациента, аллопластика – использование трупных тканей или препаратов из этих тканей, ксенопластика (гетеропластика) – использование тканей животных (пересадка тканей от особей другого биологического вида), брефопластика (от греческого brephos – плод) – аллопластика с применением тканей мертворожденных плодов или погибших новорожденных.
Показаниями к костной пластике являются дефекты костной ткани травматического и послеоперационного генеза, нарушения консолидации, деформации развившейся вследствие патологической консолидации, ортопедические заболевания – костные кисты, отдельные формы остеобластокластом, фиброзная дисплазия, последствия остеомиелита.
Использование аутогенных тканей подразумевает пересадку как свободных трансплантатов (лишённых кровоснабжения), так и трансплантатов на сосудистой ножке. Пересаживают кортикальную либо губчатую кость. Свободные трансплантаты являются матриксом для формирования на месте трансплантации новой костной ткани. При этом отмечается рассасывание пластического материала и замещение вновь сформированной костной тканью. Успех костной пластики сопряжён с синхронностью процессов рассасывания старой и формированием новой костной ткани. Костные трансплантаты на сосудистой ножке используются в расчете на полное приживление пересаженной костной ткани. При дефектах большого объёма используют комбинацию кортикальных и губчатых трансплантатов.
Под аллопластикой понимают трансплантацию трупных тканей. Возможна пересадка кортикальной и губчатой костной ткани. Наиболее часто используются кортикальные аллотрансплантаты.
Губчатые аллотрансплантаты обладают более высокой антигенной активностью, которая может привести к развитию воспаления в области пластики и секвестрации трансплантата. Это обусловлено сохранением в губчатой костной ткани элементов костного мозга, обладающего высокой антигенностью. Достаточно широко используют аллогеный деминерализованный костный матрикс – лишённая клеток и минералов белковая строма костной ткани.
При пересадке аллогенных костей, как правило, используют консервированный материал. Целью консервации материала являются стерилизация, снижение антигенности и увеличение сроков хранения пластического материала. С целью стерилизации применяют гамма излучение, химическую стерилизацию, низкие температуры и др. Хранение трансплантатов возможно в жидких, газообразных средах. Наиболее эффективна консервация пластического материала в жидких средах с одновременной стерилизацией материала, снижением антигенности и длительными сроками хранения. К таким консервантам относят жидкие среды на основе растворов формальдегида слабой концентрации.
В течение последних 30 лет сотрудники кафедры травматологии, ортопедии и ВПХ ГрГМУ под руководством проф. Болтрукевича С.И. занимались консервацией костного материала и различными видами костной пластики. Опубликовано более двухсот научных работ, защищено более десяти диссертаций. Предложена, апробирована и внедрена в практику здравоохранения новая методика консервации и стерилизации биологических тканей в слабых растворах альдегидов – формальдегида и глутарового альдегида. Указанные вещества обеспечивают консервацию и стерилизацию тканей, снижают их антигенность, сохраняя биологическую полноценность. Парабиоз и обратимость блокирования сульфгидрильных групп статических тканей позволяет хранить их в течение 12–18 месяцев. Консервированные ткани сохраняют остеоиндуктивность и бактериостатичность, что позволяет использовать их в клинической практике.
Заготовка тканей проводится у лиц, скоропостижно скончавшихся от травм, острой сердечно-сосудистой патологии, асфиксии, отравления алкоголем.
Забор материала осуществляется впервые 12 часов, перед изъятием тканей труп подвергается санитарной обработке. При заборе тканей нет необходимости в соблюдении правил асептики и антисептики. Изъятые ткани тщательно промывают проточной водой. Костная ткань освобождается от остатков мягких тканей и костного мозга.
Методика консервации костных тканей: готовят растворы 0,2–0,4% формолового и 0,1–0,2% глутарового альдегида, растворы смешивают в отношении 1:1, pН среды доводят до 7,0–7,4 путем введения фосфатного буфера 20–40 мл на литр консервирующей смеси. Приготовленный к консервации материал помещают в смесь в соотношении 1 часть материала на 5–10 частей консерванта в герметически закрывающейся стеклянной посуде. Хранение проводится в условиях бытового холодильника при t +2°–+4° по Цельсию. В течение первого месяца консервант меняют 2 раза в неделю, далее 1 раз в 1–2 месяца.
Стерилизация биологических объектов наступает в течение 6–12 часов при воздействии на них смеси растворов 0,2– 0,4% формолового и 0,1–0,2% глутарового альдегидов. Биологические ткани, консервированные в смеси ФА и ГА, подавляют рост золотистого, эпидермального стафиллококков, кишечной, синегнойной палочек и спорогенной клостридии. Выявленный синергизм действия смеси растворов формолового и глутарового альдегидов на микрофлору позволяет надежно стерилизовать заготовленные биологические ткани без соблюдения правил асептики в течение 18–72 часов и обеспечивать их устойчивость к инфекции после трансплантации в организм реципиента.
Согласно исследованиям, проведенным на кафедре травматологии, ортопедии и ВПХ ГрГМУ, решающую роль в реваскуляризации консервированных аллотрансплантатов играет сосудистое русло параоссальных тканей и окружающих мышц. Радиологическими исследованиями с помощью радионуклида кальция (45-Са) установлено, что, начиная с 2–3 недель, консервированные в смеси альдегидов кости после их трансплантации в дефекты скелета вступают в минеральный обмен. К двухнедельному сроку наблюдений изотоп регистрировался в области стыков, через месяц – в самом реплантате. Наиболее выраженное накопление зарегистрировано к 4–6 месяцам, что связано с активной перестройкой аллотрансплантата. К 6–9 месяцам содержание 45-Са в реплантированной кости постепенно снижалось, а через 12 месяцев и в более поздние сроки на всем протяжении реплантированной кости и костей ложа реципиента накопление изотопа было равномерным.
Рентгенологическими исследованиями оперированных пациентов выявлена определенная закономерность перестройки аллотрансплантатов. Так, в первом периоде (до 4 недель после операции) не определялось заметных изменений, аллотрансплантат сохранял присущую ему форму и плотность кости. Во втором периоде (1–6 месяцев после трансплантации) выявлялись признаки наличия периостальной мозоли, идущей со стороны кости реципиента. Отмечалось сращение трансплантата с костным ложем и постепенное исчезновение границы между ними. В это время происходило изменение интенсивности тени трансплантата, связанное с его частичным рассасыванием и с замещением собственной костью реципиента. Третий период (6 месяцев – 2 года) характеризуется полной консолидацией аллотрансплантата с костью реципиента и завершением окончательной перестройки костной структуры.
Ксенопластика используется достаточно редко ввиду высокой антигенности тканей. Чаще используют костный матрикс из этих материалов.
Брефоматериалы применяются также редко ввиду ограниченной доступности этого вида пластического материала.
Комбинированная пластика подразумевает совместное применение ауто- и аллотканей в различных вариантах.
Источник: Травматология и ортопедия : пособие для студентов лечебного и педиатрического факультетов / под ред. В.В. Лашковского. – Гродно
doclvs.ru
Внимание! информация на сайте не является медицинским диагнозом, или руководством к действию и предназначена только для ознакомления.
  Материал применяется только с целью обучения и ознакомления, и используется в рамках цитирования и/или как объект обсуждения.
Источник
Вследствие нарушения репаративного остеогенеза происходит замедленное сращение костей, а в некоторых случаях это приводит к их несращению и образованию ложного сустава (псевдоартроз). Причиной этого могут быть общие и местные факторы.
- Факторы нарушения заживления переломов
- Несросшийся перелом
- Псевдоартроз
- Оперативное лечение больных с ложными суставами
- Неправильное сращение кости
Факторы нарушения заживления переломов
К общим факторам относятся: нарушение функции эндокринных желез, беременность, авитаминоз, острые и хронические инфекционные заболевания, расстройства трофики т.д.
Местные факторы являются ведущими среди причин нарушения репаративного остеогенеза. Их можно разделить на три группы (Д. В. Руда, 1976):
1. Ошибки при лечении: недостаточная репозиция отломков и неустраненных интерпозиций мягких тканей между ними, ненадежная иммобилизация после репозиции и частая замена гипсовых повязок, слишком обширное скелетирование кости во время операции (нарушается кровоснабжение), применение неадекватных фиксаторов для остеосинтеза (нестабильная фиксация) и др.
2. Факторы, связанные с тяжестью травмы и ее осложнениями: множественные и открытые переломы, массивное повреждение мягких тканей (мышц, сосудов, нервов), нагноение и остеомиелит.
3. Причины, которые зависят от анатомо-физиологических особенностей перелома: локализация, степень кровоснабжения (перелом головки или шейки бедренной кости, ладьевидной кости) и другие.
Нарушение репаративного остеогенеза при переломах костей ведет к замедленной консолидации (сращения) отломков, к несращению их или образованию ложного сустава (псевдоартроз), иногда — к неоартрозу (новому суставу). Под замедленной консолидацией перелома понимают такие случаи, когда не произошло костное сращение отломков в общепринятые нормальные сроки для конкретной локализации перелома.
Несросшийся перелом
Несросшимся переломом называют такой, при котором после двойного срока, необходимого для сращивания данной кости, клинически выявляют боль и патологическую подвижность в месте перелома, рентгенологически — щель между отломками при еще закрытых (костнонезарощених) костно-мозговых полостях отломков. Если есть костная заращение этих полостей замыкающими пластинками, это говорит о сложившемся ложном суставе (псевдоартроз).
Итак, дифференцировать несросшийся перелом от псевдоартроза можно клинически за болью в месте перелома, который возникает во время движений и нагрузки конечности, и рентгенологически — за отсутствием заращениея костно-мозговых полостей.
Все последствия нарушения репаративного остеогенеза патогенетически взаимосвязаны, зависят от причинных факторов и качества лечения. Во время движения отломков происходит постоянное травмирование свежих структур костной мозоли, включая новообразованные сосуды.
При сохранении способности человеческого организма к репаративному процессу в области перелома появляются компенсаторные изменения в виде краевых разрастаний, которые в той или иной степени постепенно уменьшают патологическую подвижность отломков. Образуется гипертрофический или гиперваскулярний мозоль, при которых преобладают процессы костеобразования над процессами рассасывания кости. Несмотря на образование значительного веретенообразного загрубения в области перелома, клинически определяют патологическую подвижность, болезненность, рентгенологически костного сращения между ними не видно. Щель между отломками заполнена грубоволокнистой соединительной тканью.
Далее регенеративный процесс при замедленном сращении может идти в двух направлениях, что зависит от ряда факторов. Если отломки сжимаются между собой, а при их нагрузке (физиологическое сокращение мышц, дозированная нагрузка в повязке) действующая сила совпадает с осью поврежденного сегмента и идет перпендикулярно к линии перелома, то волокнистая соединительная ткань превращается в хрящевую, а затем — в костную, т.е. наступает вторичное сращение костей, хотя происходит оно довольно долго.
Если сила будет действовать не по оси сегмента, совпадать или приближаться к линии перелома, то кости не срастутся, и постепенно сформируется гипертрофический ложный сустав. Характерными клиническими признаками ложного сустава является патологическая подвижность и отсутствие боли на месте перенесенного перелома, рентгенологическими — закрытие костно-мозговых полостей (наличие запирающих пластинок) и щель между отломками
Преобладают процессы рассасывания костной ткани над костеобразованием. Концы отломков становятся тоньше и заостренными, а щель между ними шире. Параосальные костные наслоения исчезают. Обломки между собой соединены соединительной тканью, которая наименее дифференцированная и не требует хорошего кровоснабжения. При значительной патологической подвижности между отломками формируются щель и типичный гиповаскулярний (атрофический) псевдоартроз.
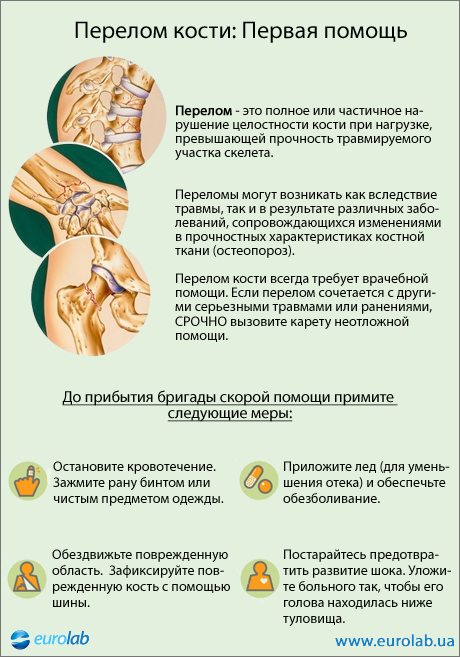
Псевдоартроз
Зачастую бывает псевдоартроз большеберцовой кости, реже — костей предплечья, плеча и бедра.
При длительном псевдоартрозе щель на время заполняется слизеподобной жидкостью, а концы отломков от трения покрываются грубоволокнистым хрящом, шлифуются, участок охватывается фиброзной капсулой и таким образом возникает новый сустав (неоартроз).
Лечение по поводу переломов костей с нарушением репаративного остеогенеза включает общие и местные средства.
Общие средства лечения заключаются в повышении имуннореактивних сил организма, тонуса мышц, улучшении гемодинамики, обменных процессов и т.д. Для этого применяют полноценное, богатое белками и витаминами, питание, анаболические стероиды (нерабол, кортикотропин), мумие, экзогенную ДНК т.д. Назначают ЛФК, массаж, физиотерапевтические процедуры (общее кварцевание, теплые укутывания и т.п.).
Местное лечение заключается в создании оптимальных условий для сращения кости путем репозиции и обездвиживания отломков, нормализации местного крово- и лимфо обращения и трофики тканей, в профилактике и рациональном лечении гнойных осложнений.
При замедленной консолидации сращения костей достигают консервативными методами — надежной фиксацией и стимуляцией репаративных процессов.
Если перелом не срастается в нормальный для него срок и сопровождается гипертрофическим мозолью, то целесообразно продолжить фиксацию сегмента гипсовой повязкой, ортезом, а лучше — аппаратом Илизарова или другим аппаратом с функциональной нагрузкой конечности. Одновременно следует применять комплекс общих и местных средств лечения, которые бы стимулировали сращения кости.
В тех случаях, когда после травмы прошло два средние сроки, необходимые для сращения кости конкретного сегмента (локализации), а сращения нет, то рассчитывать на успех консервативного лечения нельзя.
Оперативное лечение больных с ложными суставами
Оперативное лечение больных с ложными суставами применяют давно, и методы его совершенствуются по мере развития науки. При псевдоартрозе, который образовался после закрытого перелома, в свое время методом выбора был металлоостеосинтез с костной пластикой.
После обнажения участка псевдоартроз освобождают от рубцов и освежают костные отломки, которые после репозиции прочно фиксируют металлическим стержнем, убитым интрамедуллярного. Затем участок псевдоартроза перекрывают костным аутотрансплантатом, который берут из проксимального метаэпифиза большеберцовой кости или крыла подвздошной кости, используют аллотрансплантаты (консервированные трупные) или ксенотрансплантаты (бычью кость). Трансплантат тесно подгоняют губчатой поверхностью к обнаженному слою участка псевдоартроза и прочно фиксируют проволокой или болтами. Операцию заканчивают наложением гипсовой повязки, которой иммобилизуют конечность до сращивания кости.
При тугом псевдоартрозе без смещения отломков хороших результатов достигают с помощью менее травматического операции — костной пластики с Хахутовым. После обнажения участка псевдоартроз со стороны раны поднадкостничной в обоих отломков вырезают одинаковой ширины трансплантаты. Их длина в одном из отломков должна составлять 2 / с, а во втором — 1 / с общей длины трансплантата. Трансплантаты перемещают так, чтобы более длинной частью перекрыть щель псевдоартроза, а меньшей заполнить образовавшийся дефект после перемещения. После операции конечность фиксируют гипсовой повязкой до сращения кости.
При гиповаскулярном псевдоартрозе оправдала себя операция декортикации, которая обновляет процессы регенерации. После вскрытия всех мягких тканей в области псевдоартроза поднадкостничной долотом сбивают тонкие пластинки коры так, чтобы они содержались на надкостнице с прилегающими к нему мягкими тканями. Выполнив круговую декортикацию, рану зашивают и накладывают гипсовую повязку.
Для возбуждения репаративного остеогенеза и улучшения кровоснабжения участка псевдоартроз некоторые хирурги долотом делают насечки мозоли и кости на глубину 2-3 мм в виде еловой шишки. Весьма проблематично было лечение больных с инфицированным псевдоартрозом, осложненным остеомиелитом, и после открытых переломов. Лечение затягивалось на многие месяцы и даже на годы, поскольку открытое оперативное лечение можно проводить не ранее 6 месяцев после заживления нагноившейся раны или закрытия свища.
Чтобы ускорить срастание инфицированного псевдоартроза, применялась операция Стюарда-Богданова, или внеочагового обходного полисиностоза, а при дефектах большеберцовой кости — операция Гана — перемещение малоберцовой кости под большеголенную.
Разработка и воплощение в травматологическую практику компрессионно-дистракционного аппарата Илизарова открыло новую эпоху, которая в корне изменила тактику лечения при псевдоартрозах, в том числе осложненных остеомиелитом и дефектами кости.
Применение аппаратного остеосинтеза позволяет устранить деформацию, создает стабильную фиксацию поврежденного сегмента, обеспечивает движения в прилегающих суставах, позволяет нагружать конечность. Однако при гиповаскулярном псевдоартрозе процесс срастания кости даже в аппарате остается замедленным, и поэтому нужно дополнительно применять костную пластику.
Больных с нагноительных процессами в области псевдоартроза лечат по общим правилам гнойной хирургии в условиях аппаратного остеосинтеза.
При псевдоартрозах, осложненных остеомиелитом, даже когда есть свищ, применение аппарата и создание стабильной фиксации приводит к усилению регенерации, затуханию воспалительного процесса, закрытию свища и сращению кости. Если есть сформированный секвестр, проводят секвестрэктомию в аппарате или перед его наложением. С помощью аппаратного остеосинтеза удается сократить срок лечения больных и добиться сращения кости.
При дефектах кости накладывают 4-кольцевой (или больше) компрессионно-дистракционный аппарат, проводят однополюсную, а при больших дефектах — двухполюсную остеотомию (компактотомию) в метафизарном (губчатом) участке кости. После образования первичного клеточного регенерата (7-10 дней) начинают опускать средний фрагмент кости в сторону дефекта. Опускания проводят очень медленно, по 1 мм в сутки (в один или два приема по 0,5 мм), сближением между собой средних колец аппарата. По мере расширения пространства в области остеотомии он заполняется новым регенератом, постепенно растет.
При достижении сближения концов костных отломков в месте бывшего дефекта, создают некоторую их компрессию, чтобы вызвать некробиоз и стимулировать местный репаративный процесс и сращение отломков. Для полного костного сращения аппарат следует содержать в нейтральной позиции в течение 2,5-4 мес. Этот способ лечения позволяет устранять дефекты костей на значительном протяжении (15 см и более).
Неправильное сращение кости
Неправильно сросшимся называют перелом, при котором кость срослась с отклонением от ее анатомической оси и нарушением статикодинамической функции.
У больных с переломами костей, которые не лечились или неправильно лечились, кости срастаются преимущественно со смещением отломков. При неправильно сросшихся внутрисуставных переломах является инконгруентность суставных поверхностей или нарушения угловых соотношений сустава, ведет к нарушению функций конечности, контрактуры, развития посттравматического деформирующего артроза и вторичных статических деформаций.
При диафизарных переломах кости неправильно срастаются, если есть полная репозиция отломков, наложена неполноценная гипсовая повязка или ее преждевременно снят, в результате чего обломки повторно смещаются.
Очень часто отломки не управляются скелетным извлечением, когда не соблюдаются правила репозиции и не используют корригирующих тяг, или обломки вторично смещаются вследствие преждевременного снятия извлечения. Бывают случаи неправильного сращения костей, если больной нарушает режим лечения.
Лечение больных с неправильным сращиванием костей проводят тогда, когда нарушается функция конечности или имеет место укорочение нижней конечности. Укорочена верхняя конечность с сохраненной осью и функцией лечению не подлежит. Следует устранить угловое смещение отломков у детей, поскольку с возрастом деформация будет увеличиваться.
В случае неполного сращения диафизов костей деформацию можно устранить закрытым способом под наркозом. Неправильно сросшиеся диафизы и эпифизы требуют оперативного лечения. Чаще всего проводят остеотомию на верхушке деформации диафиза с фиксацией отломков металлическим фиксатором и последующим лечением, как и при свежих переломах. Сросшиеся отломки, смещены в ширину, во время операции выделяют, освежают, открывают костно-мозговые полости, а после репозиции проводят металлоостеосинтез.
Околосуставной остеотомией ограничиваются при нарушении оси конечности после внутрисуставного перелома, который обязательно требует восстановления конгруэнтности суставных поверхностей. Смещенный отломок отделяют до мозоли, репонируют под визуальным контролем и фиксируют так, чтобы совпадали суставные хрящевые поверхности. Если такая операция невозможнп, то проводят артропластику (локтевого, тазобедренного, коленного), артродез (голеностопного, коленного) или эндопротезирование (тазобедренного, коленного, локтевого суставов) у пожилых людей.
Источник
