Микроциркуляция при переломах
- Авторы
- Резюме
- Файлы
Свешников К.А., Русейкин Н.С.
У 134 больных остеопорозом и с переломами в возрасте 65-75 лет изучали состояние магистрального кровообращения после внутривенного введения альбумина человеческой сыворотки, меченного по 99мТс, а тканевой кровоток — с 133Хе. Установлено, что у здорового человека через переднюю большеберцовую мышцу протекает 0,053±0,004 мл крови на 1 г ткани в минуту. В кортикальном слое диафиза объем кровотока составлял 0,008±0,0006 мл на 1 г кости в минуту, в костном мозге — 0,030±0,002 мл/мин. На 1-2-е сутки в месте травмы кровообращение было ослаблено. С 3-х суток после травмы кровообращение начинало ускоряться во всем поврежденном сегменте (208±9,8 %). Величина капиллярного кровотока в передней большеберцовой мышце возрастала до 10,6±0,85 мл (в норме 5,3±0,42 мл). Область ускоренной циркуляции была значительно большей, чем место перелома.
Несмотря на исключительную важность состояния сосудистого русла и микроциркуляции в репаративном костеобразовании, многие аспекты этой проблемы остаются малоизученными. Установлено, что сохранение магистрального кровотока в передней большеберцовой артерии, а также внутрикостного кровотока (питательная артерия) обеспечивает кровоснабжение костной мозоли в большеберцовой кости после перелома. Функция конечности в процессе лечения восстанавливается при условии улучшения микроциркуляции в области травмы.
Материал и методы
Больных остеопорозом и с переломами в возрасте 65-75 лет обследовано 134. В эксперименте с переломами была задействована 21 собака. Состояние магистрального кровообращения у больных изучали после внутривенного введения в локтевую вену альбумина человеческой сыворотки (АЧС; фирма «CIS», Франция), меченного по 99мТс, а тканевой кровоток — с 133Хе.
Для исследования кровотока в нижних конечностях с АЧС больного помещали на стол эмиссионного фотонного компьютерного томографа (гамма-камера) — «Фо-гамма 3ЛЦ-75» фирмы «Nuclear Chicago» (США). Детектор гамма-камеры устанавливали над местом перелома с таким расчетом, чтобы в «поле зрения» попадал и симметричный участок неповрежденной конечности. Через каждые 3 секунды регистрировали время появления меченого пирофосфата в больной и неповрежденной конечностях и степень заполнения сосудов. Автоматически проводилось построение профильных кривых, характеризующих изменение активности в изучаемом отделе конечности. В итоге получали представление об объемной скорости кровотока.
При исследовании верхних конечностей больной сидел, руки помещал на стол прибора, к месту перелома и симметричному участку неповрежденной конечности приставляли детекторы установки УР-I-3 и записывали кривые накопления и выведения активности. Пространственное распределение меченого альбумина изучали путем сканирования на планисканере КЕ-32 (фирма «Radiax», Италия). Он имеет вмонтированную в прибор пересчетную радиометрическую установку, позволяющую сразу после сканирования, не изменяя положения конечности, сделать радиометрию. Ее проводили через каждые 2 см. Для получения статистически достоверных величин в каждом месте измерения подсчитывали 2000-5000 импульсов. Полученные данные сравнивали с величинами на соответствующем месте здоровой конечности.
Для исследования тканевого кровотока применяли 133Хе, растворенный в физиологическом растворе. Вводили его в объеме 0,2 мл в переднюю большеберцовую мышцу на расстоянии 8 см дистальнее нижнего края надколенника на глубину 1 см.
Число миллилитров крови (ЧМК), протекающей через мышцу, вычисляли по формуле [3]: ЧМК= 1,61Д, где Д — угол наклона кривой выведения 133Хе, 1,61 — пересчетный коэффициент, а также формуле [1]:
ЧМК = 0,693 х 0,7х100 мл на 100 г/мин,
где Т1/2 – период Т1/2 полувыведения.
В связи с тем, что в условиях клиники невозможно точно оценить состояние кровообращения непосредственно в костном мозге, в корти кальной части кости, где идет регенерация, соответствующие наблюдения сделаны в условиях эксперимента на 21 взрослой беспородной собаке (17-22 кг) при соблюдении необходимых условий [2]. У собак под наркозом (внутривенное введение пентобарбитала натрия — 30 мг/кг) с помощью аппарата Илизарова закрытым способом производили остеотомию в середине нижней трети большеберцовой кости. Затем с помощью этого же аппарата костные отломки фиксировали, создавая максимально благоприятные условия для сращения. Проксимальнее места перелома (на 1 см) в кости просверливали отверстие диаметром 2 мм для последующего введения 133Хе. Благодаря жесткой фиксации отломков собаки с первых же дней начинали передвигаться. Их обследовали на 1-й, 3-й и 7-й дни и далее еженедельно до наступления сращения и снятия аппарата.
Объем крови, протекающей через кортикальную часть большеберцовой костив месте перелома определяли с 125I-антипирином. Сущность методики сводилась к следующему. Под наркозом обнажали а.nutritia, в нее вводили тонкую иглу, соединенную с полиэтиленовой трубочкой, в которую вначале вводили 2500 ЕД гепарина, затем 0,74 МБк 125I-антипирина. После инъекции вплотную к коже приставляли два детектора установки УР-1-3 (один в верхней трети большеберцовой кости, второй — над местом перелома) и записывали кривые выведения его. После того как активность понижалась до уровня фона, в левую яремную и правую сонную артерии вставляли иглы. В яремную вену вливали 7,4 МБк 99mТс-пирофосфата. Затем через каждую минуту в течение 10 минут из сонной артерии брали по 1 мл крови. После этого производили эвтаназию животного введением 500 мг пентобарбитала натрия. Задние конечности сразу же быстро вычленяли в коленном суставе, очищали от мягких тканей и подсчитывали активность в специально созданном свинцовом домике, используя для подсчета детектор и радиометрическую установку планисканера. Далее из симметричных участков левой и правой большеберцовой костей выпиливали фрагменты длиной 6 см. В центре правого — находилось место перелома (в этих местах до вычленения проводили радиометрию). У костных фрагментов удаляли кортикальный слой, разрезали на мелкие кусочки, измельчали, определяли величину активности, а также удельную массу кости.
Величину активности в образцах крови подсчитывали на гамма-счетчике фирмы «Trakor Еuropa» (Голландия).
Кровоток в миллилитрах на 1 г кости в минуту вычисляли по формуле [4]:
где Сх(О) — максимальная величина введенной активности; Сх(t) — число импульсов за время t; Р — удельная масса кости, Stto Cx(t)dt — величина площади (в см2), определяемой на графике между кривой выведения РФП из места перелома и в неповрежденной кости; l — отношение величины активности кость/кровь для 125I-антипирина.
Величину накопления 99mТс-пирофосфата (0) определяли по формуле: 0 = В/А, где В — число импульсов в 1 г кости за 10 мин., А — число импульсов в секунду на 1 мл крови.
В костном мозге объем циркулирующей крови определяли после введения в костномозговой канал (с помощью изогнутой иглы) 3,7 МБк 133Хе. Расчет проводили по формуле [3].
Результаты исследований
Установлено, что у здорового человека через переднюю большеберцовую мышцу протекает 0,053±0,004 мл крови на 1 г ткани в минуту. В кортикальном слое диафиза объем кровотока составлял 0,008±0,0006 мл на 1 г кости в минуту, в костном мозге — 0,030±0,002 мл/мин.
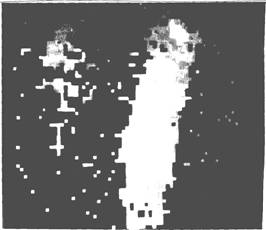
При закрытых косых и винтообразных переломах на 1-2-е сутки кровообращение в месте травмы было ослаблено. Это наглядно показано на записях компьютера гамма-камеры времени поступления меченого соединения в поврежденную конечность (рис. 1.1.-1.3). С 3-х суток после травмы кровообращение начинало ускоряться во всем поврежденном сегменте (208±9,8 %, р
| |
27 секунд после инъекции меченого пирофосфата. Уже заполнены сосуды здоровой конечности (справа). В конечности с переломом (слева) активность отсутствует | 30 секунд после инъекции. Появление активности (слева) в конечности с переломом |
| |
33 секунды после иньекции меченого пирофосфата. Дальнейшее заполнение сосудов (слева) конечности с переломом | 36 секунд после инъекции меченого пирофосфата. Активности становится больше (слева) |
Рис. 1.1. Разная скорость заполнения сосудистого русла конечности с переломом (слева) и здоровой конечности на 2-е сутки после травмы
| |
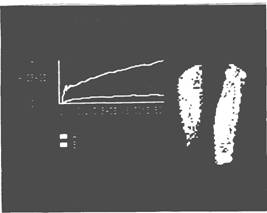
Рис. 1.2. Заполнение сосудов конечности с переломом (слева) и здоровой конечности (справа) меченым соединением на 54 с после инъекции препарата. | Рис. 1.3. Результаты компьютерной обработки данных о накоплении меченого соединения на 54 с после инъекции препарата. Верхняя кривая – данные в здоровой конечности (справа), нижняя – данные в травмированной конечности (слева) |
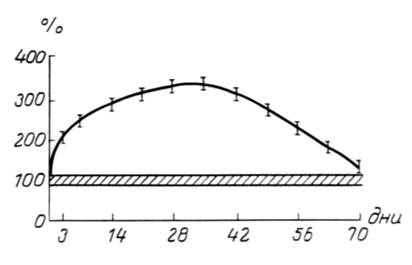
Рис. 2. Динамика кровотока в конечности при лечении переломов костей голени у больных остеопорозом (заштрихован предел колебаний в норме)
В последующие дни (42-46) величина кровотока возрастала до 240±16,3 % (р0,05), отмечены на 70-й день.
Скорость движения крови в кортикальном слое диафиза и костном мозге (исследования с 125I-антипирином и 133Хе) на различных этапах остеосинтеза отличалась: наиболее быстро она нарастала в костном мозге (рис. 3, кривая 1) и более медленными темпами в кортикальном. Максимальная величина кровотока в костном мозге была на 5-й день. После этого уменьшалась, наиболее заметно к 14-му дню. Дальнейшее возвращение к норме происходило более медленными темпами, а полная нормализация — к 70-му дню.
В кортикальном слое места перелома максимальная величина кровотока установлена на 14-й день (ускорение в 7,5 раз) и он сохранялся на высоком уровне до 23-го дня. Возвращение к норме происходило медленнее, чем в костном мозге, а полная нормализация отмечена на 90-й день (рис.3, кривая 2).
На значительном удалении от места перелома (верхняя треть голени) также отмечалось ускорение кровообращения, но было оно значительно менее выражено (1,7 раза) и менее продолжительным (первые 3 недели после травмы).
Рис. 3. Состояние кровооб ращения в костном мозге (1) и в месте сращения отломков (2). Динамику костеобразо вания отражает кривая 3 (заштрихован предел колебаний в норме)
Накопление меченого остеотропного препарата (пирофосфата) увеличивалось однонаправлено с изменением кровотока в кортикальном слое кости: вначале отмечено значительное увеличение с максимальными значениями (в 7 раз) на 15-й день (рис. 3, кривая 3). Высокий уровень накопления наблюдался в течение первого месяца после травмы. В дальнейшем, как и при исследовании кровообращения, происходило медленное понижение накопления РФП с полной нормализацией к 90-му дню.
Таким образом, в области перелома наблюдалось непрерывное усиление кровообращения, достигавшее наибольших значений на 5-й неделе. В этот же период происходило интенсивное костеобразование, о чем свидетельствовали результаты с меченым пирофосфатом и рентгенологические данные. Тенденция к ослаблению кровотока наблюдалась на 6-й неделе, что указывало на достаточную зрелость регенерата и прочность сращения.
СПИСОК ЛИТЕРАТУРЫ:
1. Коркушко О.В., Саркисов К.Г., В.Э.Фрейдефельд. // Мед. радиол. 1988. № 9. С. 39.
2. Проведение исследований на биомоделях и на лабораторных животных // Режим доступа: https://www.consilium-medicum.com/media.book.05_01/24.shtml.
3. Kety S. S. // Am. Heart. J. 1949. V. 38. P. 321.
4. Paradis G.R., Kelly P.J. // J. Bone Jt. Surg. 1975. V. 57A. P. 220.
Библиографическая ссылка
Свешников К.А., Русейкин Н.С. МИКРОЦИРКУЛЯЦИЯ ПРИ РЕПАРАТИВНОМ ПРОЦЕССЕ ПОСЛЕ ПЕРЕЛОМОВ У БОЛЬНЫХ ОСТЕОПОРОЗОМ // Современные проблемы науки и образования. – 2008. – № 2.;
URL: https://science-education.ru/ru/article/view?id=685 (дата обращения: 02.06.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Переломы костей конечностей сопровождаются отчетливыми нарушениями капиллярного кровообращения без существенных изменений тонуса магистральных сосудов. Нарушения микроциркуляции при переломах носят разнонаправленный характер и зависят от локализации и тяжести повреждения, времени, прошедшего с момента травмы, возраста больного, способа лечения и длительности иммобилизации. В 60 % случаев причинами нарушения кровообращения в области перелома являются повреждения вен либо их осложнения. Нарушения микроциркуляции в области перелома приводят к ишемическому синдрому и, как следствие, — замедлению репаративных процессов.
Микротромбозы плохо проявляются клинически, не позволяют достоверно определить уровень, характер и эмбологенность поражения, но оказывают существенное влияние на сроки консолидации и вероятность развития инфекционных осложнений. Выраженные расстройства регионарного кровотока в месте перелома костей приводят к усилению выпотевания плазмы в фасциальные футляры конечностей, образованию стойких плотных отеков, способных вызывать прекращение кровообращения, развитие ишемии, а затем и некроз тканей.
В клинической практике при лечении переломов посттравматические сосудистые нарушения часто не учитываются, что может существенно повлиять на сроки и исходы лечения.
С созданием и применением низкомолекулярных гепаринов появились новые возможности в профилактике микротромбозов и повышения эффективности лечения переломов костей.
Анализ современной отечественной и зарубежной литературы, данные собственных клинических наблюдений позволили обосновать необходимость профилактики тромбоэмболических осложнений у больных с повреждениями опорно-двигательной системы, а также при оперативных вмешательствах на тубчатых костях и крупных суставах.
Превентивные меры следует относить к неотложным мероприятиям, проводимым по жизненным показаниям у всех пострадавших с ограничением подвижности при повреждениях костей конечностей. В профилактике тромбозов вен различают специфические и неспецифические мероприятия.
Неспецифическая профилактика основана на активизации кровообращения и устранении застойных явлений крови в нижних конечностях, стимуляции фибринолиза воздействием физических факторов.
Специфическая профилактика воздействует на отдельные этапы гемокоагуляции. Убедительно доказана высокая эффективность в профилактике тромбоэмболических осложнений у пострадавших с переломами костей низкомолекулярных декстранов (гепаринов), которые воздействуют на сосудисто-тромбоцитарный этап гемостаза. Низкомолекулярные декстраны уменьшают агрегационные свойства тромбоцитов и эритроцитов, повышают эндогенный фибринолиз, воздействуют на макрогемодинамику, компенсируя гиповолемию и гемодилюцию.
Важную роль в профилактике тромбоэмболических осложнений играют препараты, угнетающие агрегацию тромбоцитов — антиагреганты, которые не угнетают синтез физиологических антикоагулянтов.
Эффективность прямых и непрямых антикоагулянтов не вызывает сомнений, они значительно уменьшают вероятность тромбозов. Однако применение этих препаратов связано с угрозой повышения кровоточивости тканей, требует осторожности и динамического лабораторного контроля за состоянием свертывающей системы крови.
Создание низкомолекулярных гепаринов открыло новые возможности в профилактике тромбозов и связанных с ними осложнений.
Низкомолекулярные гепарины отличаются более продолжительным эффектом, не требуют необходимости в ежедневном лабораторном контроле, а побочные осложнения развиваются значительно реже.
Для профилактики развития тромбозов при лечении пострадавших со скелетной травмой разработан алгоритм применения специфических и неспецифических мероприятий в зависимости от степени риска.
При хирургическом лечении переломов костей таза, позвоночника, нижних конечностей, крупных суставов, множественной и сочетанной травмы низкомолекулярные гепарины являются препаратами выбора.
Опыт клинического применения низкомолекулярных гепаринов (клексан, фраксипарин, фрагмин) при хирургическом лечении 480 пострадавших с переломами костей голени, бедренной кости, крупных суставов, множественными и сочетанными переломами костей конечностей подтвердил высокую эффективность предупреждения сосудистых тромбозов и связанных с ними осложнений. Их применение отличалось простотой, удобством и надежностью. Уменьшилось число инфекционных осложнений в 1,5-1,8 раза. Нормализация регионарного кровообращения в поврежденном сегменте предупреждала развитие отеков, ишемию тканей и благоприятно влияла на репаративные процессы, снижала риск развития тромбоэмболии легочной артерии и тромбозов вен в 2 раза.
Высокая эффективность, хорошая переносимость и безопасность низкомолекулярных гепаринов позволяет считать их применение оправданным и целесообразным при хирургическом лечении переломов костей. Раннее начало, комплексная и последовательная профилактика тромбоэмболических осложнений, своевременное выявление и лечение развивающихся осложнений способны уменьшить летальность, повысить эффективность лечения и улучшить качество жизни пациентов.
В. П. Хомутов, Ю. В. Гудзь
Центр стабильно-функционального остеосинтеза Елизаветинской больницы, кафедра военной травматологии и ортопедии ВМА, г. Санкт-Петербург
Опубликовал Константин Моканов
Источник
Сложившиеся в настоящее время представления о заживлении переломов и микроциркуляции во многом противоречивы и носят преимущественно описательный характер. Отсюда следует, что эту проблему необходимо рассматривать с позиций системного подхода к пониманию многоуровневой организации опорно-двигательного аппарата, определяющей порядок взаимодействия и основные специфические свойства этих уровней. В настоящее время выделены следующие, связанные между собой уровни организации аппарата опоры и движения:
клеточный уровень специализированных структурно-функциональных элементов или капиллярно-тканевых систем;
органный уровень непосредственно взаимодействующих органов;
организменный уровень или уровень целостного опорно-двигательного аппарата.
На клеточном уровне осуществляются регулируемые генетическим аппаратом метаболические функции специализированных клеток и их взаимодействие через клеточные мембраны с внутренней средой, обеспечивающей метаболические потребности клеток, а, следовательно, и условия их жизнедеятельности в составе капиллярно-тканевых систем.
«Чрескостный остеосинтез в травматологии», В.И.Стецула, А. А. Девятов
Капиллярно-тканевые системы представляют собой сложившиеся в процессе индивидуального развития специализированные структурно-функциональные элементы органов, состоящие из клеток и основного вещества нескольких тканей и связанные между собой посредством путей микроциркуляции крови и тканевой жидкости, нервных волокон и их окончаний. Эти системы пространственно ограничены бассейном кровоснабжения артериол. Условия нормальной жизнедеятельности капиллярно-тканевых систем и их специализированных клеточных элементов обеспечиваются …
Быстро возникающие функционально-необратимые нарушения тканевого гомеостаза резко нарушают условия жизнедеятельности и приводят к дезорганизации капиллярно-тканевых систем, что при полном прекращении циркуляции жидкости может заканчиваться их гибелью. При сохранении проходимости микроциркуляторного русла в результате его расширения создаются условия для возобновления микроциркуляции и проявления способности капиллярно-тканевых систем к самовосстановлению, которое неизбежно проходит фазы острых циркуляторных нарушений, дезорганизации, …
На уровне непосредственно взаимодействующих органов различных отделов аппарата опоры и движения и их частей, связанных ветвями магистральных периферических сосудов и нервов, осуществляются 2 взаимосвязанных вида межорганного взаимодействия: прямое механическое взаимодействие костей и мышц; гемодинамическое взаимодействие, которое значительно увеличивает возможности перераспределения тока крови и еще больше повышает функциональную лабильность, а, следовательно, и надежность кровоснабжения органов. На …
В каждом участке зоны, вовлеченной в репаративный процесс, отмечается одинаковая последовательность изменений, составляющих 4 фазы репаративной реакции или репаративного цикла. I — фаза функционально необратимых нарушений микроциркуляции. Сопровождается циркуляторной гипо- и аноксией, накоплением метаболитов, повышением проницаемости стенок капилляров и возникновением белкового отека. II — фаза дезорганизации капиллярно-тканевых систем. Проявляется набуханием структурных элементов с разрушением межклеточных …
Направление дифференцировки незрелой скелетогенной ткани в регенерате определяется не только гистогенетическими потенция ми, но и во многом зависит от местной микроциркуляции. Интенсивная микроциркуляция, обеспечивающая высокий уровень напряжения кислорода, приводит к созданию оптимальных условий для новообразования кости. При низкой интенсивности микроциркуляции и напряжения кислорода клетки скелетогенной ткани дифференцируются в фибробласты, продуцирующие волокнистую соединительную ткань, а в …
Продолжительность фаз и циклов перестройки по сравнению с репаративным циклом значительно увеличена, а полициклическое течение перестройки обеспечивает периодическую смену генерации остеобластов, что и является причиной формирования пластинчатой кости. Отсюда следует, что регенерация кости является сложным и разнородным восстановительным процессом, в котором необходимо различать репаративную реакцию и процесс перестройки, так как они связаны с различными уровнями …
При репаративной реакции и перестройке новообразование кости всегда неразрывно связано с остеокластической резорбцией, хотя соотношения между ними очень сильно варьируют. Учитывая, что при переломах костей репаративная реакция отличается от медленно протекающей перестройки кости и регенерата локальной интенсивной пролиферацией скелетогенной ткани и бурным новообразованием грубоволокнистых костных балочек, можно считать, что с прекращением прогрессирования репаративного эндостального и …
Изучение зависимости между функциональной нагрузкой и перестройкой кости позволило установить, что под влиянием динамического компонента функциональной нагрузки в костях возникают упругие деформации, создающие выраженные гидродинамические эффекты, которые, оказывая влияние на микроциркуляцию, являются необходимым фактором обеспечения нормальной трофики и сохранения структурной организации костей, адекватно действующей на них среднесуточной функциональной нагрузки (В. И. Стецула и соавт., 1983). …
При переломах костей местные травматические нарушения микроциркуляции всегда сочетаются с расстройствами внутрикостного и регионарного кровообращения, что связано с нарушениями функциональных и анатомических соотношений между непосредственно взаимодействующими органами из-за выключения функции поврежденной конечности. Эти нарушения кровообращения приводят к активизации перестройки костной ткани поврежденной кости, обусловливающей появление посттравматического остеопороза различной степени выраженности. Тщательная репозиция и стабильная фиксация …
Источник