Атипичный перелом что это
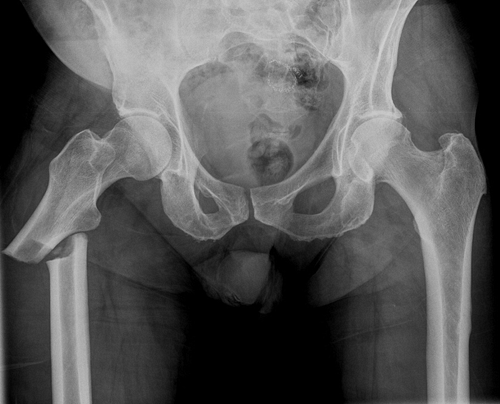
Atypical femoral fractures mimicking metastatic lesions in 2 patients taking denosumab
Источник: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5434608/
75-летняя женщина с историей метастатической молочной железы и немелкоклеточного рака легких сработала и упала на ее бедро. Рентгенограммы показали правый диафрагмальный перелом бедренной кости и пациент подвергался антероградной интрамедуллярной фиксации (рис. 1А). Рак молочной железы пациента был метастатическим в левое подвздошное крыло и позвоночный позвонок. Она получала ежемесячные инъекции denosumab в течение предыдущих 2 лет, чтобы помочь контролировать ее метастатическое заболевание, и отрицала наличие каких-либо предшествующих симптомов. Несмотря на то, что не было доказательств злокачественности при гистологическом анализе интраоперационных реанимаций, впервые предполагалось, что перелом возник из-за метастатического поражения. В ретроспективе первоначальный перелом имел вид атипичного перелома бедренной кости (AFF). Пациент продолжал дезосумаб, и ее правый перелом бедренной кости исцелился, но через 8 месяцев у нее появилось коварное прерывистое боль в ее левом бедре. Пациентка посетила своего онколога после 1 месяца симптомов, после чего были проведены рентгенограммы и сканирование кости, чтобы исключить злокачественность (рисунок 1B). Сканирование костей показало повышенную активность левого дистального диафиза бедренной кости. На следующий день после сканирования пациент упал, и рентгенограммы выявили левый дистальный третильный бедренный перелом, показывающий атипичные особенности, включая боковое корковое утолщение, для которого она прошла ретроградную интрамедуллярную фиксацию (рис. 1С).
Пациент 1. A. Правильная бедренная кость; начальный атипичный перелом. B. Получение изображений с помощью костей, полученных для оценки наличия метастатического заболевания, демонстрируя повышенное поглощение в левом дистальном диафизе бедра. Это поглощение указывало на стрессовые изменения в кости до завершения атипичного перелома бедренной кости. C. Ретроградная интрамедуллярная фиксация ногтей.
86-летний мужчина с историей метастатического рака предстательной железы упал, и рентгенограммы показали правый поперечный диафрагмальный перелом бедренной кости с боковым корковым утолщением, согласующийся с атипичным переломом (рис. 2А). Пациентка лечилась антероградным интрамедуллярным гвоздем, а гистология интраоперационных исследований была отрицательной для злокачественности. Пациент начал ежемесячное лечение denosumab за 3,5 года до перелома для лечения метастатического заболевания в области таза и позвоночника. За год до перелома пациент отметил правильную боль в бедре и рентгенограмму, сделанную за 5 месяцев до того, как перелом показал боковое корковое утолщение диафиза его бедренной кости (рис. 2B). Сканирование костей во время этой радиографии показало повышенное поглощение, и поражение было признано метастатическим заболеванием (рисунок 2C). Пациент был оценен ортопедическим хирургом, который оценил его как метастатическое поражение, и за этим последовало местное облучение бедра. За 1 месяц до травмы и после завершения лучевой терапии пациент был замечен для ортопедического наблюдения и продолжал сообщать о боли в бедрах, но дальнейшее вмешательство не проводилось.
Пациент 2. А. Правая бедренная кость; атипичный перелом. B. Правая бедренная кость после того, как у пациента развилась боль в бедрах, показана боковое кортикальное утолщение диафиза. C. Образцы сканирования костей, полученные для оценки наличия метастатического заболевания, демонстрирующие повышенное поглощение в правом среднем диафизе бедра. Первоначально это поглощение представляло собой метастатическое заболевание, хотя в конечном итоге оно подтвердило наличие изменений напряжения в костях перед завершенным атипичным переломом бедра.
Антирезорбтивные препараты, прежде всего бисфосфонаты, используются для лечения остеопороза и для лечения боли, связанной с метастатическим заболеванием кости. Возможным осложнением антирезорбтивных лекарств является нетипичный перелом бедренной кости (AFF), который чаще всего встречается в бедренном валу (Koeppen 2013). Бисфосфонаты связываются с кристаллами гидроксиапатита в костном матриксе, что в конечном итоге приводит к снижению резорбции кости (Drake et al., 2008). Хотя это может привести к улучшению плотности костной ткани, оно также нарушает нормальный гомеостатический баланс между остеобластами и остеокластами. Это изменение может привести к накоплению микро-повреждений и, в конечном счете, к AFF (Mashiba et al., 2000, Visekruna et al., 2008). Истинное заболевание этих атипичных переломов у пациентов с бисфосфонатным препаратом было трудно установить (Schilcher et al., 2015).
Denosumab — это недавно разработанное человеческое моноклональное антитело, которое связывается с рецепторным активатором каппа-B-лиганда ядерного фактора (RANK-L), предотвращая созревание, активацию и выживаемость остеокластов (Rizzoli et al., 2010). Он получил одобрение FDA в 2010 году для профилактики скелетных осложнений у пациентов с метастазами в кости и для лечения женщин в постменопаузе с остеопорозом. Хотя denosumab функционирует по другому механизму, чем бисфосфонаты, оба уменьшают резорбцию кости. Первоначальные результаты исследования FREEDOM, рандомизированное исследование denosumab у 7 868 женщин, не выявили никаких AFF у участников (Cummings et al., 2009). Последующее расширение FREEDOM отмечало только 2 AFF во время лечения с общей частотой менее 1 перелома на 10 000 исследуемых лет (Bone et al., 2013, Papapoulos et al., 2015). В исследованиях фазы III, оценивающих использование denosumab для метастатического скелетного заболевания и множественной миеломы, также не сообщалось ни о каких AFF (Lipton et al., 2012). В последнее время в отчетах стало известно, что denosumab, как и бисфосфонаты, может привести к развитию AFF (Paparodis et al., 2013, Villiers et al., 2013, Drampalos et al., 2014, Schilcher and Aspenberg 2014, Thompson et al., 2014, Khow and Yong 2015, Selga et al., 2016). Мы представляем 2 случая, когда пациенты развивали АФФ при одновременном приеме denosumab для метастатического рака и в которых продромальные симптомы считались прежде всего связанными с новыми метастатическими поражениями и не были вторичными по отношению к развивающимся переломам. Мы получили информированное письменное согласие обоих пациентов на публикацию этого отчета.
6 отчетов о случаях привели убедительные доказательства того, что AFF могут быть связаны с использованием denosumab для остеопороза (Villiers et al., 2013, Drampalos et al., 2014, Schilcher and Aspenberg 2014, Thompson et al., 2014, Khow and Yong 2015, Selga et al. 2016). Во всех предыдущих случаях были описаны AFF, которые наблюдались у женщин, получавших denosumab в течение двух лет для лечения остеопороза. У наших 2 пациентов, по-видимому, развились атипичные переломы бедра, а при месячном лечении деносумабом при метастатической злокачественности. Пациенты, получающие denosumab для минимизации скелетных осложнений, связанных с метастатическим раком, получают более высокое дозирование (120 мг против 60 мг) и более частое дозирование (ежемесячно или два раза в год), чем пациенты, проходящие лечение, связанное с остеопорозом (Lipton et al., 2012, Papoulos et al. 2015). Пациенты с AFF в предыдущих отчетах имели предыдущую терапию бисфосфонатом, тогда как пациенты, описанные в этом случае, не имели такого воздействия. Ранее отмечались атипичные переломы бедренной кости у пациентов с высокой дозой бисфосфонатной терапии злокачественных новообразований (Puhaindran et al., 2011). Насколько нам известно, ранее не было сообщений о пациентах, поддерживающих AFF, при лечении denosumab для метастатического заболевания.
Наши пациенты выдержали AFF 2, 3 и 3,5 года после начала терапии denosumab. Эти интервалы времени до перелома больше, чем в предыдущих отчетах, которые отмечали переломы после 1 недели до 18 месяцев лечения (Paparodis et al., 2013, Villiers et al., 2013, Drampalos et al., 2014, Schilcher and Aspenberg 2014, Thompson et al. 2014, Khow and Yong 2015, Selga et al., 2016), но на эти предыдущие отчеты, возможно, повлияло использование предыдущего бисфосфоната. Исследование AFF с высокодозовой бисфосфонатной терапией для злокачественности показало среднюю продолжительность лечения 6 лет (Chang et al., 2012), что было значительно больше, чем у наших пациентов.
Переломы, наблюдаемые у наших пациентов, соответствовали критериям AFF в соответствии с Целевой группой Американского общества костей и минералов 2013 года (Shane et al., 2014), поскольку они были расположены в бедренном диафизе и удовлетворяли всем 5 основным критериям, включая: низкоэнергетические механизмы, происходящие из боковой коры, с участием обеих коры, как правило, не расщепляются и демонстрируют локализованное периостальное или эндостальное утолщение боковой коры. Левый перелом бедренной кости, наблюдаемый у первого пациента (рис. 1C), по-видимому, был самым дистальным индуцированным denosumab AFF, зарегистрированным до сих пор, требующим ретроградного гвоздя, сохраняя при этом классические отличительные черты AFF.
Как и у нашего первого пациента, в предыдущих докладах были отмечены высокая частота двустороннего участия связанных с denosumab AFFs с одним случаем одновременных переломов (Selga et al., 2016), 2 случая с одновременными изменениями (Villiers et al., 2013, Thompson et al. 2014) и 1 случай последовательных AFF, приблизительно на один год (Drampalos et al., 2014). Аналогичные данные были получены у пациентов, получавших лечение бисфосфонатом с высокой дозой для скелетных метастазов, причем 5 из 6 пациентов показали двустороннее участие в одной серии (Chang et al., 2012). У нашего пациента первоначальный перелом не был признан в то время как AFF, и он был признан ретроспективно только во время второго перелома. Точно так же начальное кортикальное утолщение, боль в бедре и повышенное поглощение при сканировании костей у второго пациента были неправильно диагностированы как метастатическое заболевание даже после ортопедической оценки. У пациента, получающего лечение denosumab для метастатического рака, диагностический дифференциал для боли в бедрах должен включать атипичный перелом бедренной кости, который может потребовать прекращения приема лекарств и ограничений веса или профилактической фиксации.
Источник
Справочник болезней
«Знание некоторых принципов легко заменяет незнание некоторых фактов» Гельвеций
ОПРЕДЕЛЕНИЕ
Остеопороз — заболевание скелета, для которого характерны снижение прочности кости и повышение риска переломов.
МОРФОЛОГИЯ
Нормальная кость. Остеопороз.
ФАКТОРЫ РИСКА ОСТЕОПОРОЗА
• Возраст >65 лет.
• Снижение минеральной плотности кости.
• Индекс массы тела <20 кг/м² или вес <57 кг.
• Женщины.
• Дефицит половых гормонов: ранняя менопауза, гистерэктомия, овариэктомия.
• Курение.
• Недостаточное потребление кальция (в норме 1000–1500 мг/сут).
• Дефицит витамина D (в норме 400–800 МЕ/сут).
• Злоупотребление алкоголем.
• Низкая физическая активность.
• Иммобилизация.
• Другие заболевания: диабет, ревматоидный артрит, ХБП 4–5 стадий.
• Медикаменты: прием кортикостероидов >3 мес.
КЛИНИКА ОСТЕОПОРОЗА
• Снижение роста на ≥2 см за 1–3 года.
• Увеличение грудного кифоза.
• Острая боль в спине при физической работе, резких движениях, кашле, повороте в постеле, мануальной терапии.
• Хроническая боль в спине, крупных костях, усиливается при нагрузке, тряске, уменьшается лежа.
ПОКАЗАНИЯ К ДЕНСИТОМЕТРИИ (ISCD)
• Женщины ≥65 лет.
• Женщины в постменопаузе в возрасте <65 лет с факторами риска переломов.
• Мужчины в возрасте ≥70 лет.
• Мужчины моложе 70 лет c факторами риска переломов.
• Взрослые, перенесшие переломы при небольшой травме.
• Взрослые с заболеваниями, ассоциирующимися с низкой костной массой или костными потерями.
• Взрослые, принимающие медикаменты, которые ассоциируются со снижением костной массы или костными потерями.
• Пациенты, которым планируется лечение остеопороза.
• Пациенты, которым проводится терапия остеопороза, для оценки эффекта лечения (не ранее 5 летнего курса, ACP).
Двухэнергетическая рентгеновская абсорбциометрия (DXA)
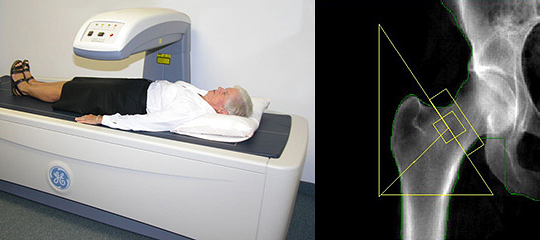
КЛАССИФИКАЦИЯ МИНЕРАЛЬНОЙ ПЛОТНОСТИ КОСТЕЙ
• Норма: T-критерий +2.5 −1 стандартных отклонений от пиковой костной массы.
• Остеопения: T-критерий −1 до −2.5 стандартных отклонений.
• Остеопороз: T-критерий −2.5 стандартных отклонений и ниже.
• Тяжелый остеопороз: −2.5 стандартных отклонений и ниже с наличием одного и более переломов.
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
• Общий кальций, фосфор.
• Паратиреоидный гормон.
• 25(ОН)D3.
• Креатинин, скорость клубочковой фильтрации.
• Тиреотропный гормон.
ФОРМУЛИРОВКА ДИАГНОЗА
• Идиопатический остеопороз. [M81.5]
• Сенильный остеопороз, множественные переломы тел грудных позвонков. [M80.8]
• Ревматоидный артрит, серонегативный. Глюкокортикоидный остеопороз, компрессионный перелом Th9.
• Остеопороз постменопаузальный, тяжелый (Т −2.8), компрессионные переломы Th7, Th10, закрытый перелом шейки левого бедра (2018, 2020). Тромбоз глубоких вен бедра, легочная эмболия. [M80.0]
ПОКАЗАНИЯ К МЕДИКАМЕНТОЗНОМУ ЛЕЧЕНИЮ ОСТЕОПОРОЗА (NOF)
• Переломы позвоночника (асимптомные или симптомные) или переломы бедра.
• Двухэнергетическая рентгеновская костная абсорбциометрия бедра или остистых отростков позвонков с Т-критерием ≤−2.5.
• Остеопения и 10-летняя вероятность перелома бедра ≤3% или 10-летняя вероятность любых переломов, связанных с остеопорозом, ≤20%.
• Предпочтение пациентов с 10-летним риском переломов ниже вышеуказанных уровней.
ОБЩИЕ РЕКОМЕНДАЦИИ ПАЦИЕНТАМ С ОСТЕОПОРОЗОМ (NOF)
• Динамические физические нагрузки: ходьба.
• Упражнения по ношению тяжестей, укреплению мышц.
• Предупреждение падений.
• Отказ от курения, избыточного потребления алкоголя.
• Избегать нагрузки с прыжками, падениями.
• Диета с достаточным количеством кальция (1000 мг/сут, дозы >1000–1500 мг/сут могут повысить риск сердечно-сосудистых болезней, мочевых камней).
• Протекторы бедра.
• Препараты кальция, витамин D3.
Атипичный (подвертельный) перелом бедренной кости при лечении бифосфонатами

Подвертельный или диафизарный, поперечный или короткий наклонный, нет связи с травмой, отсутствие дробления.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ ОСТЕОПОРОЗА
• Бифософнаты: аледронат, ибандронат, ризедронат, золедроновая кислота — лечение до 3–5 лет в связи с рисками (атипичный перелом бедра, остеонекроз нижней челюсти, рак пищевода [FDA, EMA]).
• Моноклональные антитела к RANKL, склеростину: деносумаб, ромосозумаб.
• Паратиреоидный гормон: терипаратид.
ПРЕДУПРЕЖДЕНИЕ ПАДЕНИЙ
• Медикаменты: избегать медикаментов, провоцирующих падения (бензодиазепины, трициклические антидепрессанты, диуретики, дигидропиридины, ИАПФ, нитраты).
• Заболевания: лечение заболеваний, вызывающих падения (костномышечные, глазные, неврологические, вестибулярные…).
• Физическая активность: сохранять физическую активность, упражнения с плавными движениями (ходьба, в воде, тай-чи).
• Адекватная обувь: прочная, нескользящая и нетолстая подошва, адекватный размер, на шнурках туго затянутых.
• Домашняя обстановка: убрать провода, коробки, мебель с проходов, закрепить напольные покрытия, расположить одежду, посуду, продукты для удобного доступа, нескользящие коврики в ванной.
• Жизненное пространство: ночники в спальне, коридорах и ванной, удобный доступ к выключателям света (с подсветкой в темноте).
• Вспомогательные средства: поручни с обеих сторон лестницы, нескользящие ступеньки, унитаз с поручнями, прочные пластиковые сиденья и поручни в ванной.
Источник
Atypical femoral fractures mimicking metastatic lesions in 2 patients taking denosumab
Источник: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5434608/
75-летняя женщина с историей метастатической молочной железы и немелкоклеточного рака легких сработала и упала на ее бедро. Рентгенограммы показали правый диафрагмальный перелом бедренной кости и пациент подвергался антероградной интрамедуллярной фиксации (рис. 1А). Рак молочной железы пациента был метастатическим в левое подвздошное крыло и позвоночный позвонок. Она получала ежемесячные инъекции denosumab в течение предыдущих 2 лет, чтобы помочь контролировать ее метастатическое заболевание, и отрицала наличие каких-либо предшествующих симптомов. Несмотря на то, что не было доказательств злокачественности при гистологическом анализе интраоперационных реанимаций, впервые предполагалось, что перелом возник из-за метастатического поражения. В ретроспективе первоначальный перелом имел вид атипичного перелома бедренной кости (AFF). Пациент продолжал дезосумаб, и ее правый перелом бедренной кости исцелился, но через 8 месяцев у нее появилось коварное прерывистое боль в ее левом бедре. Пациентка посетила своего онколога после 1 месяца симптомов, после чего были проведены рентгенограммы и сканирование кости, чтобы исключить злокачественность (рисунок 1B). Сканирование костей показало повышенную активность левого дистального диафиза бедренной кости. На следующий день после сканирования пациент упал, и рентгенограммы выявили левый дистальный третильный бедренный перелом, показывающий атипичные особенности, включая боковое корковое утолщение, для которого она прошла ретроградную интрамедуллярную фиксацию (рис. 1С).
Пациент 1. A. Правильная бедренная кость; начальный атипичный перелом. B. Получение изображений с помощью костей, полученных для оценки наличия метастатического заболевания, демонстрируя повышенное поглощение в левом дистальном диафизе бедра. Это поглощение указывало на стрессовые изменения в кости до завершения атипичного перелома бедренной кости. C. Ретроградная интрамедуллярная фиксация ногтей.
86-летний мужчина с историей метастатического рака предстательной железы упал, и рентгенограммы показали правый поперечный диафрагмальный перелом бедренной кости с боковым корковым утолщением, согласующийся с атипичным переломом (рис. 2А). Пациентка лечилась антероградным интрамедуллярным гвоздем, а гистология интраоперационных исследований была отрицательной для злокачественности. Пациент начал ежемесячное лечение denosumab за 3,5 года до перелома для лечения метастатического заболевания в области таза и позвоночника. За год до перелома пациент отметил правильную боль в бедре и рентгенограмму, сделанную за 5 месяцев до того, как перелом показал боковое корковое утолщение диафиза его бедренной кости (рис. 2B). Сканирование костей во время этой радиографии показало повышенное поглощение, и поражение было признано метастатическим заболеванием (рисунок 2C). Пациент был оценен ортопедическим хирургом, который оценил его как метастатическое поражение, и за этим последовало местное облучение бедра. За 1 месяц до травмы и после завершения лучевой терапии пациент был замечен для ортопедического наблюдения и продолжал сообщать о боли в бедрах, но дальнейшее вмешательство не проводилось.
Пациент 2. А. Правая бедренная кость; атипичный перелом. B. Правая бедренная кость после того, как у пациента развилась боль в бедрах, показана боковое кортикальное утолщение диафиза. C. Образцы сканирования костей, полученные для оценки наличия метастатического заболевания, демонстрирующие повышенное поглощение в правом среднем диафизе бедра. Первоначально это поглощение представляло собой метастатическое заболевание, хотя в конечном итоге оно подтвердило наличие изменений напряжения в костях перед завершенным атипичным переломом бедра.
Антирезорбтивные препараты, прежде всего бисфосфонаты, используются для лечения остеопороза и для лечения боли, связанной с метастатическим заболеванием кости. Возможным осложнением антирезорбтивных лекарств является нетипичный перелом бедренной кости (AFF), который чаще всего встречается в бедренном валу (Koeppen 2013). Бисфосфонаты связываются с кристаллами гидроксиапатита в костном матриксе, что в конечном итоге приводит к снижению резорбции кости (Drake et al., 2008). Хотя это может привести к улучшению плотности костной ткани, оно также нарушает нормальный гомеостатический баланс между остеобластами и остеокластами. Это изменение может привести к накоплению микро-повреждений и, в конечном счете, к AFF (Mashiba et al., 2000, Visekruna et al., 2008). Истинное заболевание этих атипичных переломов у пациентов с бисфосфонатным препаратом было трудно установить (Schilcher et al., 2015).
Denosumab — это недавно разработанное человеческое моноклональное антитело, которое связывается с рецепторным активатором каппа-B-лиганда ядерного фактора (RANK-L), предотвращая созревание, активацию и выживаемость остеокластов (Rizzoli et al., 2010). Он получил одобрение FDA в 2010 году для профилактики скелетных осложнений у пациентов с метастазами в кости и для лечения женщин в постменопаузе с остеопорозом. Хотя denosumab функционирует по другому механизму, чем бисфосфонаты, оба уменьшают резорбцию кости. Первоначальные результаты исследования FREEDOM, рандомизированное исследование denosumab у 7 868 женщин, не выявили никаких AFF у участников (Cummings et al., 2009). Последующее расширение FREEDOM отмечало только 2 AFF во время лечения с общей частотой менее 1 перелома на 10 000 исследуемых лет (Bone et al., 2013, Papapoulos et al., 2015). В исследованиях фазы III, оценивающих использование denosumab для метастатического скелетного заболевания и множественной миеломы, также не сообщалось ни о каких AFF (Lipton et al., 2012). В последнее время в отчетах стало известно, что denosumab, как и бисфосфонаты, может привести к развитию AFF (Paparodis et al., 2013, Villiers et al., 2013, Drampalos et al., 2014, Schilcher and Aspenberg 2014, Thompson et al., 2014, Khow and Yong 2015, Selga et al., 2016). Мы представляем 2 случая, когда пациенты развивали АФФ при одновременном приеме denosumab для метастатического рака и в которых продромальные симптомы считались прежде всего связанными с новыми метастатическими поражениями и не были вторичными по отношению к развивающимся переломам. Мы получили информированное письменное согласие обоих пациентов на публикацию этого отчета.
6 отчетов о случаях привели убедительные доказательства того, что AFF могут быть связаны с использованием denosumab для остеопороза (Villiers et al., 2013, Drampalos et al., 2014, Schilcher and Aspenberg 2014, Thompson et al., 2014, Khow and Yong 2015, Selga et al. 2016). Во всех предыдущих случаях были описаны AFF, которые наблюдались у женщин, получавших denosumab в течение двух лет для лечения остеопороза. У наших 2 пациентов, по-видимому, развились атипичные переломы бедра, а при месячном лечении деносумабом при метастатической злокачественности. Пациенты, получающие denosumab для минимизации скелетных осложнений, связанных с метастатическим раком, получают более высокое дозирование (120 мг против 60 мг) и более частое дозирование (ежемесячно или два раза в год), чем пациенты, проходящие лечение, связанное с остеопорозом (Lipton et al., 2012, Papoulos et al. 2015). Пациенты с AFF в предыдущих отчетах имели предыдущую терапию бисфосфонатом, тогда как пациенты, описанные в этом случае, не имели такого воздействия. Ранее отмечались атипичные переломы бедренной кости у пациентов с высокой дозой бисфосфонатной терапии злокачественных новообразований (Puhaindran et al., 2011). Насколько нам известно, ранее не было сообщений о пациентах, поддерживающих AFF, при лечении denosumab для метастатического заболевания.
Наши пациенты выдержали AFF 2, 3 и 3,5 года после начала терапии denosumab. Эти интервалы времени до перелома больше, чем в предыдущих отчетах, которые отмечали переломы после 1 недели до 18 месяцев лечения (Paparodis et al., 2013, Villiers et al., 2013, Drampalos et al., 2014, Schilcher and Aspenberg 2014, Thompson et al. 2014, Khow and Yong 2015, Selga et al., 2016), но на эти предыдущие отчеты, возможно, повлияло использование предыдущего бисфосфоната. Исследование AFF с высокодозовой бисфосфонатной терапией для злокачественности показало среднюю продолжительность лечения 6 лет (Chang et al., 2012), что было значительно больше, чем у наших пациентов.
Переломы, наблюдаемые у наших пациентов, соответствовали критериям AFF в соответствии с Целевой группой Американского общества костей и минералов 2013 года (Shane et al., 2014), поскольку они были расположены в бедренном диафизе и удовлетворяли всем 5 основным критериям, включая: низкоэнергетические механизмы, происходящие из боковой коры, с участием обеих коры, как правило, не расщепляются и демонстрируют локализованное периостальное или эндостальное утолщение боковой коры. Левый перелом бедренной кости, наблюдаемый у первого пациента (рис. 1C), по-видимому, был самым дистальным индуцированным denosumab AFF, зарегистрированным до сих пор, требующим ретроградного гвоздя, сохраняя при этом классические отличительные черты AFF.
Как и у нашего первого пациента, в предыдущих докладах были отмечены высокая частота двустороннего участия связанных с denosumab AFFs с одним случаем одновременных переломов (Selga et al., 2016), 2 случая с одновременными изменениями (Villiers et al., 2013, Thompson et al. 2014) и 1 случай последовательных AFF, приблизительно на один год (Drampalos et al., 2014). Аналогичные данные были получены у пациентов, получавших лечение бисфосфонатом с высокой дозой для скелетных метастазов, причем 5 из 6 пациентов показали двустороннее участие в одной серии (Chang et al., 2012). У нашего пациента первоначальный перелом не был признан в то время как AFF, и он был признан ретроспективно только во время второго перелома. Точно так же начальное кортикальное утолщение, боль в бедре и повышенное поглощение при сканировании костей у второго пациента были неправильно диагностированы как метастатическое заболевание даже после ортопедической оценки. У пациента, получающего лечение denosumab для метастатического рака, диагностический дифференциал для боли в бедрах должен включать атипичный перелом бедренной кости, который может потребовать прекращения приема лекарств и ограничений веса или профилактической фиксации.
